食物與健康
 健康飲食
健康飲食 【福島食品真的NG嗎?3】輻射其實無所不在
星期五, 25 2月 2022 12:01已故知名科學家居禮夫人曾說:「Nothing in life is to be feared. It is only to be...
推薦>>精選文章
健康資訊庫

 |
羅德島州普羅維登斯2019年10月24日 /美通社/ -- 羅氏集團旗下成員公司日本中外製藥株式會社(Chugai Pharmaceutical Co., Ltd.)今天宣佈,將延長公司對EpiVax, Inc.(簡稱「EpiVax」)開發的免疫原性篩選和蛋白質重組介面(ISPRI)工具包的授權存取權限。
擁有生物技術產品優勢的日本領先的研究型製藥公司之一日本中外製藥,在2013年9月延長與其他矽工具的頭對頭比較之後,將先進的ISPRI工具包集成到其臨床前評估系列中。此次延期三年將使兩家公司的業務關係延續到2022年,標誌著ISPR使用了9年,有力地證明了EpiVax免疫資訊學工具的準確性和實用性。
ISPRI包含幾種專門演算法,有助於評估免疫原潛能和減少候選藥物產生不良影響的可能性,從而提高成功開發的機會。ISPRI支持新的生物製品與一系列天然人類蛋白質的比較,並考慮到Tregitopes(調節性T細胞表位)對免疫原性潛力的影響。Tregitopes是由EpiVax發現的一種自然免疫系統「關閉開關」,其功能是降低對高變蛋白質的免疫原性。日本中外製藥是目前在臨床開發前授權篩選生物製劑的工具的12家大型製藥公司之一。
日本中外製藥研究人員已經用ISPRI工具包篩選了成千上萬的生物序列,找到了一些創新療法,如一種新型的抗C5回收抗體SKY59,一種開創性的抗血友病A的雙特異性抗體Hemlibra以及許多其它療法。日本中外製藥全資研究子公司Chugai Pharmabody Research Pte. Ltd.行政總裁Tomoyuki Igawa博士表示:「我們期待著在我們的抗體和蛋白質藥物發現中繼續有效地使用EpiVax工具。感謝與日本中外製藥的持續業務關係。我們期待著公司在未來幾年推出更多創新生物製品。」
EpiVax簡介
總部位於羅德島的生物技術公司EpiVax開發了一個安全、互動式的網路免疫原性篩選工作環境ISPRI。ISPRI可用於部分和完整的蛋白質治療候選序列的高通量篩選,以鑒定潛在的免疫原性區域(表位元簇),並精細地映射那些對該簇的免疫原性貢獻最大的各個氨基酸。ISPRI是考慮了與調節性T細胞誘導相關的獨特的EpiVax發現Tregitopes的唯一篩選工具。EpiVax為ISPRI工具包頒發許可證並進行定制分析,為世界各地許多大型製藥公司和小型生物技術公司提供服務。有關EpiVax的更多資訊,請瀏覽http://www.epivax.com。
日本中外製藥簡介
日本中外製藥是日本領先的研究型製藥公司之一,在生物技術產品方面具有優勢。公司總部設在東京,日本中外製藥專門經營處方藥,並在東京證券交易所第一部上市。作為羅氏集團的重要成員之一,日本中外製藥積極參與日本內外的研發工作。日本中外製藥正在開發創新產品,以滿足未滿足的醫療需求。更多資訊,請瀏覽https://www.chugai-pharm.co.jp/english。
聯繫人:
醫學博士Anne De Groot
電郵:
電話: (401) 272-2123
手機: (401) 952-4227
圖標 - https://mma.prnewswire.com/media/542055/EpiVax_Logo.jpg
蘇州2019年10月21日 /美通社/ -- 信達生物製藥(香港聯交所股票代碼:01801),一家致力於研發、生產和銷售用於治療腫瘤、自身免疫和代謝疾病等重大疾病的創新藥物的生物製藥公司,今天宣佈,由Incyte發起的pemigatinib治療復發的晚期膽管癌患者II期臨床試驗的最新陽性結果在2019年歐洲腫瘤內科學會(ESMO)上進行了報告。
2018年12月,信達生物與Incyte就Incyte發現並研發的三個臨床試驗階段候選藥物達成戰略合作,包括pemigatinib(FGFR1/2/3抑制劑,已獲美國食品藥品監督管理局(FDA)的「突破性療法認定」)、itacitinib(JAK1抑制劑)和parsaclisib(PI3Kδ抑制劑)。根據協議條款,信達生物獲得了在中國大陸、中國香港、中國澳門和中國台灣地區對這三個候選藥物在血液病和腫瘤治療領域進行開發和商業化的權利。
在2019年ESMO上報告的該II期FIGHT-202試驗的最新研究結果,包括主要終點指標的最終結果。該試驗旨在評價pemigatinib(一種成纖維細胞生長因子受體(FGFR)選擇性抑制劑)治療既往經治療的局部晚期或轉移性膽管癌患者的療效。在FGFR2基因融合或重排的患者中(隊列A),pemigatinib單藥治療後的總體緩解率(ORR)為36%(主要終點),中位隨訪15個月時的中位無進展生存期(PFS)為6.9個月(次要終點)。pemigatinib的總體耐受性良好。
這些數據為Incyte計劃在2019年底前向美國食品藥品監督管理局(FDA)提交有關pemigatinib的新藥申請(NDA)提供了支撐。
膽管癌是一種發生於膽管的惡性腫瘤。根據其起源部位可以分為肝內膽管癌(iCCA)和肝外膽管癌。膽管癌患者通常在診斷時已處於疾病後期或晚期,預後較差。膽管癌的發病率存在區域性差異,北美和歐洲地區的發病率為0.3 ~ 3.4/100,000。FGFR2基因融合或重排幾乎僅發生於iCCA,其中10% ~ 16%的患者存在這種情況。
FIGHT-202研究的主要結果
在ESMO上報告的該研究的最新數據顯示,在既往經治的局部晚期或轉移性膽管癌伴FGFR2基因融合或重排的患者中(隊列A,n=107),pemigatinib單藥治療後,基於獨立中心影像評估的確證的總體緩解率(ORR)為36%,其中3例患者出現完全緩解(CR),35例患者出現部分緩解(PR)。在這些患者中,疾病控制率(DCR)達82%,中位緩解持續時間(DOR)達7.5個月,中位無進展生存期(PFS)達6.9個月。初步的中位總生存期(OS)達21.1個月,試驗數據振奮人心。但由於這些數據尚不成熟,隨訪將繼續進行。
FIGHT-202研究中各隊列的總體緩解率(ORR)、緩解持續時間(DOR)、疾病控制率(DCR)和無進展生存期(PFS)
|
|
隊列A FGFR2基因融合或重排 |
隊列B 其他FGF/FGFR基因突變 |
隊列C 無FGF/FGFR基因突變 |
|
|
(N = 107) |
(N = 20) |
(N = 18) |
|
ORR,%(95%CI) |
|
0 |
0 |
|
|
|
0 |
0 |
|
最佳OR,n(%) |
35 PR(33) |
0 |
0 |
|
|
50 SD(47) |
8 SD(40) |
4 SD(22) |
|
中位DOR,月(95% CI) |
|
- |
- |
|
DCR,%(95%CI) |
|
40(19-64) |
22(6-48) |
|
中位PFS,月(95% CI) |
|
2.1(1.2-4.9) |
1.7(1.3-1.8) |
|
中位OS,月(95%CI) |
|
6.7(2.1-10.6) |
4.0(2.3-6.5) |
|
NE:不可評價 註:1例患者的FGF/FGFR狀態未獲得中心實驗室確認,該患者被納入安全性分析,但未被分配至任何療效評價隊列。 |
該安全性分析納入了146例患者,結果顯示pemigatinib的總體耐受性良好。最常見的治療期不良事件(TEAE)為1級或2級高磷血症(60%),採用低磷飲食、使用磷結合劑和利尿劑、或在減量或暫停用藥後均可得到控制。最常見的≥3級TEAE為低磷血症(12%);這些事件均非嚴重不良事件,且均未導致藥物減量或停藥。在4%的患者中觀察到漿液性視網膜脫離(≥3級,1%),但均未導致臨床後遺症。
關於FIGHT-202
FIGTT-202 II期、開放性、多中心研究(NCT02924376)旨在評價pemigatinib(成纖維細胞生長因子受體(FGFR)選擇性抑制劑)在既往經治的且FGF/FGFR狀態已明確的局部晚期或轉移性膽管癌成人(年齡≥18歲)患者中的安全性和療效。
受試者將進入三個隊列中的一個:隊列A(FGFR2基因融合或重排)、隊列B(其他FGF/FGFR基因突變)或隊列C(無FGF/FGFR基因突變)。所有患者均接受pemigatinib 13.5 mg口服給藥,每日1次(QD),以21天為一週期(給藥2周/停藥1周),直至出現影像學疾病進展或不可接受的毒性。
FIGTT-202的主要終點為隊列A中獨立審查委員會根據RECIST v1.1評估的總體緩解率(ORR)。次要終點包括隊列B的ORR、隊列A與B的總體ORR,以及隊列C的ORR;以及所有隊列的無進展生存期(PFS)、總生存期(OS)、緩解持續時間(DOR)、疾病控制率(DCR)和安全性。
如需瞭解更多有關FIGHT-202的信息,請訪問:
https://clinicaltrials.gov/ct2/show/NCT02924376
關於FIGHT
FIGHT(FIbroblast Growth factor receptor in oncology and Hematology Trial,有關成纖維細胞生長因子受體在實體腫瘤和血液腫瘤中的臨床試驗)的臨床試驗項目包括正在進行的II期和III期研究,這些研究評價了pemigatinib在多種FGFR驅動的惡性腫瘤中的安全性和療效。 II期單藥治療研究包括FIGHT-202以及FIGHT-201研究,後者評價了pemigatinib在轉移性或手術不可切除(包括FGFR3基因突變或融合/重排陽性)的膀胱癌患者中的療效;FIGHT-203研究針對FGFR1基因融合/重排的髓系/淋巴系血液腫瘤患者;FIGHT-207研究針對既往經治的FGFR基因突變或融合/重排的局部晚期/轉移性或不可手術切除的惡性實體瘤患者(不考慮腫瘤類型)。FIGHT-205是一項II期研究,旨在評價pemigatinib與派姆單抗聯合治療和pemigatinib單藥治療在既往未經治療且不適合接受順鉑治療的FGFR3基因突變或融合/重排的轉移性或不可切除的膀胱癌患者中的療效。FIGHT-302是一項近期啟動的III期研究,旨在評價pemigatinib作為一線治療在FGFR2基因融合/重排膽管癌患者中的療效。
關於FGFR和Pemigatinib
成纖維細胞生長因子受體(FGFR)在腫瘤細胞增殖、存活、遷移和血管生成(新血管的形成)中發揮重要作用。FGFR基因融合/重排、易位和擴增極可能導致多種癌症的發生。
pemigatinib是一種由Incyte發現和研發的、針對FGFR亞型1/2/3的強效選擇性口服抑制劑,在臨床前研究中已證實該藥物對FGFR基因突變的腫瘤細胞具有選擇性的藥理學活性。pemigatinib已獲得美國食品藥品監督管理局(FDA)「突破性療法認定」,用於治療既往經治的晚期/轉移性或不可切除的FGFR2基因易位型膽管癌。FDA的「突破性療法認定」旨在加快用於嚴重疾病治療藥物的開發和審評進程,其條件是這些藥物已顯示出鼓舞人心的早期臨床效果,而且療效可能相較現有藥物具有實質性的改善。
關於信達生物
「始於信,達於行」,開發出老百姓用得起的高質量生物藥,是信達生物的理想和目標。信達生物成立於2011年,致力於開發、生產和銷售用於治療腫瘤、自身免疫、代謝疾病等重大疾病的創新藥物。2018年10月31日,信達生物製藥在香港聯合交易所有限公司主板上市,股票代碼:01801。
自成立以來,公司憑借創新成果和國際化的運營模式在眾多生物製藥公司中脫穎而出。建立起了一條包括21個新藥品種的產品鏈,覆蓋腫瘤、自身免疫、代謝疾病等多個疾病領域,其中4個品種入選國家「 重大新藥創製 」專項,16個品種進入臨床研究,4個品種進入臨床III期研究,3個單抗產品上市申請被國家藥品監督管理局受理,並均被納入優先審評,1個產品 (信迪利單抗注射液,商品名:達伯舒®,英文商標:Tyvyt®)獲得國家藥品監督管理局批准上市,獲批的第一個適應症是復發/難治性經典型霍奇金淋巴瘤。
信達生物已組建了一支具有國際先進水平的高端生物藥開發、產業化人才團隊,包括眾多海歸專家,並與美國禮來製藥、Adimab、Incyte和韓國Hanmi等國際製藥公司達成戰略合作。信達生物希望和大家一起努力,提高中國生物製藥產業的發展水平,以滿足百姓用藥可及性和人民對生命健康美好願望的追求。詳情請訪問公司網站:www.innoventbio.com。
如需瞭解更多信息,敬請聯繫:
媒體:
郵件:
電話:+86 512-69566088
投資者:
郵件:
電話:+86 512-69566088
日內瓦2019年10月18日 /美通社/ -- Marine在彎腰幫助殘疾母親時脊椎骨折。Lo Lan在被家裏一塊松軟的地毯絆倒後摔斷了髖骨。

Osteoporosis causes bones to become weak and easily breakable, resulting in life-changing fractures. Older adults who are alert to their possible osteoporosis risk factors can take steps for timely prevention by asking for testing and treatment if needed.
這兩位女性都有一個共同點。她們都不知道自己患有骨質疏松症,這種疾病會導致骨骼變得脆弱,像玻璃一樣易碎。即便是在站著時發生最輕微的摔倒,或是打噴嚏/彎腰系鞋帶,骨質疏松症病人也會發生骨折。
全球50歲或以上人群,每三個女性、每五位男性中就有一人會因骨質疏松而骨折。大約2億人受到影響,每3秒就造成一例骨折。
在10月20日的世界骨質疏松日(World Osteoporosis Day),國際骨質疏松基金會(International Osteoporosis Foundation ,簡稱IOF)及其全球250個成員組織敦促所有老年人了解骨質疏松症的危險因素,如果有風險要咨詢醫生。
雖然有許多因素指向可能患有骨質疏松症,其中最常見的是:50歲以上的人在低創傷後骨折;身高下降超過4厘米(約1.5英吋);長期使用糖皮質激素和其他骨質破壞藥物;身體虛弱和體重不足;以及父母有骨質疏松或髖部骨折的病史。參加新的網上IOF骨質疏松症風險檢查(IOF Osteoporosis Risk Check),是一個審視可能的骨質疏松症風險快速和簡單方法。
晚年骨折會改變生活。常見的有劇烈疼痛、長期康複、長期殘疾、對照料者的依賴以及生活質量的喪失。髖部骨折可能危及生命,幸存者的能力和獨立性嚴重喪失,40%不能獨立行走,60%一年後需要幫助。由於喪失這些能力,33%的人在髖部骨折後完全依賴他人或住在療養院。
IOF主席Cyrus Cooper教授說:
「所有成年人都必須把骨骼健康作為優先事項。保持強健的骨骼和肌肉是晚年主動、靈活的關鍵。如果有患病風險,必要時應該毫不猶豫地向你的醫生詢問測試和適當的治療策略。如今,有一系列有效的骨質疏松症治療方法被證明可以將髖部骨折的風險降低40%,把脊柱骨折的風險降低30-70%。」
IOF還呼籲衛生當局優先重視骨骼健康,從而減輕其國家因脆弱性骨折造成的昂貴的人力和經濟負擔。
Cooper教授補充道:「作為這一領域的專家,我們與病人倡導共同敦促全球采取行動。普遍存在的治療缺口使得即使是最高危的病人也無法預防骨折。已經發生過一次脆弱性骨折的人很容易再骨折,在第一年內發生另一次骨折的風險是前者的五倍。然而,這些病人中大約有80%的人既未被確定也未接受骨折根本原因——骨質疏松症的治療。」
解決治療缺口和全球脆弱性骨折危機的一個關鍵策略是在所有接診骨折病人的醫院實施骨折聯絡服務(Fracture Liaison Services)。這種協同、多學科的服務改善了病人護理,有助於減少繼發性骨折,最終降低了全球與骨折相關的巨大醫療成本。
關於世界骨質疏松日(WOD)
這項活動在每年10月20日舉行,旨在呼籲全球采取行動,在全球範圍內防治骨質疏松症和相關骨折。網址:www.worldosteoporosisday.org
WOD官方合作夥伴:Sunsweet、武田製藥(Takeda)、美敦力(Medtronic)
關於IOF
國際骨質疏松基金會是世界上最大的致力於骨骼健康和骨質疏松預防的非政府組織。請在社交媒體上關注@iofbonehealth,網址:www.iofbonehealth.org
傳媒聯繫人:L.Misteli,電郵:
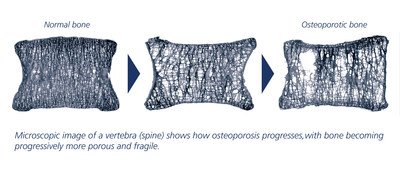
With osteoporosis, bones become progressively more porous and fragile. People with osteoporosis can fracture a bone because of a minor fall from standing height, a bump, or even from bending to tie a shoelace.
圖片 - https://mma.prnewswire.com/media/1005044/IOF_risks_Infographic.jpg
圖片 - https://mma.prnewswire.com/media/1005045/IOF_osteoporotic_bone_changes.jpg
 |
威斯康辛州沃特福德2019年10月17日 /美通社/ -- Avidity Science欣然宣佈,該公司已完成對Edstrom Japan Ltd的收購。這項收購將助推Avidity Science建立全球業務版圖,為研究工具市場提供支持。
Edstrom Japan總部位於日本東京,30多年來,一直為日本生態缸研究市場提供廣泛的產品和服務解決方案。除了為Avidity Science水淨化產品組合提供支持外,Edstrom Japan還提供各種用於生物醫學研究的設備、消耗品和服務。
Avidity Science行政總裁Doug Lohse表示:「透過收購Edstrom Japan,我們將擴大在亞洲與客戶的互動及合作,推動我們實現成為重要市場中更有價值的研究工具合作夥伴的目標。這是我們朝著利用科學提高生活質量的使命邁出的又一步。」
Avidity Science大亞洲區董事總經理Yasuto Tamukai表示:「我們很高興能借助Edstrom Japan的能力,在日本提供優質產品和服務。」
Avidity Science簡介
Avidity Science是為科研和醫療機構提供水淨化系統和實驗室設備的全球領導者。自1969年成立以來,該公司憑藉獨特的水淨化與輸送、環境監測和服務解決方案,確立了在實驗室研究市場的領導地位。詳情請瀏覽該公司網站:www.AvidityScience.com。
圖標 - https://mma.prnewswire.com/media/716246/Avidity_Science_Logo.jpg
印尼雅加達2019年10月17日 /美通社/ -- 印尼領先的醫療健康超級應用Alodokter已完成3300萬美元C輪融資。本輪融資由Sequis Life領投,飛利浦、Heritas Capital、Hera Capital、Dayli Partners等公司參投。現有投資者軟銀風投亞洲公司和Golden Gate Ventures也參與了本輪融資。
Alodokter是印尼領先的健康平台,每月活躍用戶超過2000萬,這使其成為全球最值得信賴的健康科技服務之一。Alodokter首席執行官Nathanael Faibis表示:「印尼的醫療體繫在過去10年裡發生了巨大的變化,比起更成熟的市場,印尼更熱衷於擁抱數字創新。印尼正成為全球最先採用數字原生醫療體系的國家之一。這是我們自推出以來實現超高速增長的關鍵因素之一。」
如今,患者使用Alodokter與醫生聊天、預約看病、發現定制化內容並管理健康保險。Alodokter正在與一個由20000名醫生以及1000家醫院和診所組成的可信賴網絡合作。Alodokter聯合創始人Suci Arumsari說:「找到合適的醫療信息、合適的醫生和合適的財務解決方案,對印尼各地的家庭來說極其重要。我是Alodokter的典型用戶,作為兩個孩子的母親,我的醫學知識卻很有限。在管理家庭健康狀況方面,Alodokter改變了我的生活。我們希望成為所有印尼家庭的守護天使」
Alodokter利用生態系統推動新健康保險迅速增長
Alodokter將利用這筆資金擴大其醫院網絡的整合,並進一步發展其尖端健康保險服務。2018年,該公司推出了一項名為「Alodokter Protection」的健康保險。保單持有人可以直接在APP中購買、支付和理賠。他們還可以使用一系列高級服務,例如無限次在線咨詢和優先訪問醫院。該公司正在建立「21世紀的保險」,該保險不僅提供財務保護,還引導患者在治病過程中採用合適的醫療解決方案。
印尼的私人健康保險市場基本處於未開發的階段,滲透率不足2%,僅為鄰國馬來西亞的十分之一。大多數印尼中產階級家庭仍因為意外的醫療費用,而面臨很高的破產風險。隨著用戶發現Alodokter簡單實惠的保險產品,保險銷售額在過去6個月裡猛增15倍。
Sequis Life總裁、董事兼首席執行官Tatang Widjaja表示:「除了他們的用戶群之外,其強大的醫療DNA以及為患者提供端到端解決方案的清晰願景也給我們留下了深刻的印象。Alodokter正在成為印尼醫療體系的基石,我們很自豪能為他們的發展獻一份力。我們將攜手合作,進一步實現我們發掘新技術和新流程以及印尼未開發的細分市場和客戶的目標。」
Alodokter簡介:
Alodokter是印尼領先的醫療健康超級應用,由Nathanael Faibis和Suci Arumsari於2014年創建。Alodokter為患者提供了一種端到端數字解決方案,包括遠程醫療、醫生預約、醫療內容和健康保險服務,每月為超過2000萬用戶提供服務。
圖片 - https://photos.prnasia.com/prnh/20191016/2612600-1?lang=2
Too many connections [1040]
An sql error occurred while fetching this page. Please contact an administrator if this problem persists.
新澤西州普林斯頓2019年10月15日 /美通社/ -- 全球數碼品牌保護和產品認證技術領導者Systech今天宣佈,該公司發佈新的Systech Brand Protection Suite™(Systech品牌保護套件),這個完全集成的平台將會與造假者進行鬥爭,解決產品被非法轉銷的問題,並能遵守監管法規。
在這裡體驗互動式多渠道新聞稿:https://www.multivu.com/players/zh/8471153-systech-launches-new-systech-brand-protection-suite/
新套件是當前唯一能夠將品牌保護的四大支柱 -- 序列化、可追溯性、認證和營運洞察分析 -- 結合到一起的整體解決方案。Systech所能提供的改進後的解決方案,採用該公司備受讚譽的e-Fingerprint®(電子指紋)技術,以便將非附加身份驗證與無縫追蹤和報告能力結合到一起。該套件利用簡單的包裝條碼,讓品牌所有者能夠就具體產品在供應鏈中的流通情況,獲得端到端可視性和可促成行動的數據驅動型洞察分析。
新套件所擁有的新功能包括:
- 在用戶透過智能手機對採用e-Fingerprint技術留下「電子指紋」印記的產品進行驗證時,能夠向他們推送獨一無二的信息和穩固內容
- 在UniSecure®流動軟件開發工具包(SDK)上提供有所改進的界面
- 全面支持新的俄羅斯醫藥序列化監管要求
- 憑藉提供Verification Router Service(驗證路由器服務),對遵守美國食品藥品監督管理局(FDA)關於《藥物供應鏈安全法案》(DSCSA)的已退貨藥物再次出售規定,予以支持
- 為特別報告和商業分析,進入強大的包裝線、序列化、聚合和供應鏈數據庫
Systech行政總裁Ara Ohanian表示:「以強有力的方式將我們的品牌保護套件的各個元素彙集到一起很有必要,每個元素都能為滿足客戶需求提供至關重要的價值。將產品序列化、可追溯性、數碼化認證和我們所能提供的連接性結合到一起,在市場上無與倫比。此次發佈新產品突出表明了我們對於不斷在品牌保護上面實現創新的客戶承諾。」
Systech提供數碼產品認證和可追溯性解決方案,以打擊假冒偽劣、防止產品被非法轉銷和滿足合規要求。依託數十年作為藥品序列化領導者的經驗,我們的全面品牌保護套件提供了應對供應鏈威脅所需的即時洞察、可付諸行動的產品數據、數碼連接和消費者互動功能。
各行各業的全球性品牌依靠我們來確保從製造到傳遞到消費者手中,其產品都是真實無偽、安全且聯網的。我們一起徹底改革品牌保護!
傳媒聯繫人:
市場推廣副總裁Jefferson Barr
電話:+1-609-235-8446
電郵:
圖標 - http://mma.prnewswire.com/media/461585/Systech_Logo.jpg



