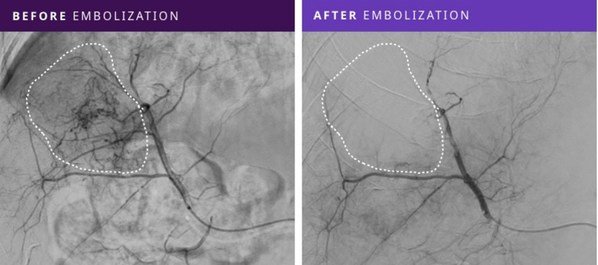
-潛在的多中心研究評估使用聚乙二醇液體栓塞劑治療高血管腫瘤的安全和有效性
麻省貝德福德2022年3月16日 /美通社/ -- Instylla, Inc. 是一家私營公司,旨在開發治療外周血管栓塞的下一代液體栓塞劑,今天在 Journal of Vascular and Interventional Radiology(《血管和介入放射學期刊》簡稱 JVIR)公佈試驗結果i 該結果是來自用於治療多血管腫瘤的 Embrace™ 水凝膠栓塞劑系統 (HES) 的首次人體臨床試驗。這項潛在的、單組多中心研究表明,在研究中接受治療的所有八名患者中,如 30 天的跟進影像所示,Embrace HES 透過阻斷腫瘤血液供應,有效栓塞惡性和良性多血管腫瘤,並取得技術成功和持續栓塞i。
阿爾弗雷德醫院介入放射科主管、澳洲墨爾本莫納什大學副教授及本研究主要作者 Gerard Goh 博士評論道:「Embrace HES 在一系列高血管腫瘤栓塞中的第 I 期首次人體研究顯示出有前景的結果 。Embrace HES 具有巨大的潛力,它易於使用、在所有患者中取得技術成功,並且在 30 天的跟進影像中沒有顯示腫瘤血運重建。
對 8 名患有多種腫瘤類型的患者進行了 10 次栓塞,包括肝細胞癌 (HCC)、肝內膽管癌 (ICC) 和血管平滑肌脂肪瘤 (AML)。腫瘤大小介乎 2.1 至 7.5 厘米不等,用 0.4 至 4.0 毫升的 Embrace HES 治療,平均用藥時間為 15 分鐘。
台灣高雄醫科大學附屬醫院內科教授 Jee-Fu Huang 博士補充說:「台灣地區是東亞地區經年齡調整的發病率最高的地區之一,這也是癌症相關死亡的第二大原因。這種新型液體栓塞劑旨在實現毛細血管水平栓塞ii,在首次人體研究試驗(包括首次人體研究腫瘤)中具有良好的患者預後。我們對這些結果感到鼓舞。我們的中心目前正參加 Instylla HES HVT 關鍵研究,因此我期待繼續評估 Embrace HES 在治療多血管腫瘤方面的功用。」
關於 Embrace 水凝膠栓塞劑系統:
Embrace HES 是一種研究裝置,旨在用於栓塞血管中 5 毫米及以下的多血管腫瘤。Embrace HES 由兩種低黏度液體前體組成,它們在輸送到血管中時會凝固,形成一種軟水凝膠,在栓塞過程中填充血管腔。Embrace HES 栓塞術不使用溶劑,不需要根據血管直徑確定尺寸,並且消除了導管卡住的可能性。其主要成分是水和聚乙二醇 (PEG)。
關於 Instylla:
Instylla, Inc. 是一家位於麻省貝德福德的私營公司,專注開發用於介入放射學的下一代液體栓塞劑,初步臨床應用在介入腫瘤學和外周止血。公司的第一款產品 Embrace HES 專為在這些臨床條件下設計受控、全面和持久的栓塞。Instylla 由 Incept LLC 於 2017 年創立,由多家領先的風險投資集團資助。
如欲了解更多資訊,請瀏覽:https://www.instylla.com/
i Gerard S. Goh, Mark D. Goodwin, Jee-Fu Huang, Helen Kavnoudias, Andrew Holden, A Phase I First in Human Study of Embrace™ a Polyethylene Glycol Based Liquid Embolic in the Embolization of Malignant and Benign Hypervascular Tumors (Embrace™ 的第 I 期人體研究:一種基於聚乙二醇、用於栓塞惡性和良性多血管腫瘤的液體栓塞劑), Journal of Vascular and Interventional Radiology (《血管和介入放射學期刊》), 2022, ISSN 1051-0443, https://doi.org/10.1016/j.jvir.2022.02.021。
ii Ganguli S, Lareau R, Jarrett T, Soulen MC, A Water-based Liquid Embolic: Evaluation of Safety and Efficacy in a Rabbit Kidney Model (基於水質的液體栓塞:在兔腎模型的安全性和有效性評估), Journal of Vascular and Interventional Radiology (《血管和介入放射學期刊》) (2021), doi: https://doi.org/10.1016/j.jvir.2021.02.018
注意:研究性器材。受聯邦(或美國)法律限制,僅限用於研究。不可出售。